Оксид меди (i)
Содержание:
- Коррозия меди в воде
- Чистка монет из меди
- Чистка монет из меди
- Сварка меди и её сплавов со сталью. Как сваривать медь и сталь
- 1 Что такое коррозия металлов и сплавов?
- Как обычное железо превращается в «нержавейку»
- Коррозийные свойства меди
- Историческая справка, характеристика меди
- Химические свойства хрома
- При каких условиях начинается разрушение алюминия на воздухе
- Коррозийные свойства
- Что такое коррозия металлов и сплавов
- Нахождение в почве и влажном воздухе
- Новые бессвинцовые сплавы
- Окисленная медь
- Кабели из катодной меди: применение
- Что такое коррозия металлов и сплавов
- Коррозия луженой меди
Коррозия меди в воде
Скорость коррозии меди в воде во многом зависит от наличия на поверхности оксидных пленок.
В быстро движущихся водных растворах и воде медь подвергается такому виду разрушения, как ударная коррозия. Скорость протекания ударной коррозии меди сильно зависит от количества растворенного кислорода. Если вода сильно аэрирована – ударная коррозия меди протекает интенсивно, если же обескислорожена – разрушение незначительно. Коррозия меди в аэрированной воде усиливается с уменьшением рН, увеличением концентрации ионов хлора. Скорость коррозии меди в воде зависит от климатической зоны. В тропиках скорость разрушения несколько выше.
Особенностью меди, омываемой морской водой, можно считать то, что она является одним из немногих металлов, которые не подвержены обрастанию микроорганизмами. Ионы меди для них губительны.
С чистой меди очень часто изготавливают трубопроводы для подачи в дома воды. Они надежны, служат очень долгое время. При наличии в воде растворенной угольной и других кислот медь понемногу корродирует, а продукты коррозии меди окрашивают сантехническое оборудование. Если вода, проходящая через медные трубы контактирует с железом, алюминием или оцинкованной сталью – то коррозию этих металлов значительно усиливается. Ионы меди осаждаются на поверхности этих металлов, образуя коррозионные гальванические элементы.
Чтоб исключить вредное влияние воды с медных труб на другие металлы используют луженую медь. Внутреннюю часть медного трубопровода покрывают оловом. Оловянное покрытие должно быть безпористым, во избежание возникновения гальванического элемента (олово по отношению к меди является катодом).
Чистка монет из меди
Медные монеты представляют собой антиквариат, и в наше время не выпускаются. Нередко их приходится чистить, чтобы вернуть привлекательный вид. Если монета контактировала со свинцом, налет на ней может быть желтоватым. В таком случае он прекрасно очищается столовым уксусом (9%). Зеленый налет убирают раствором лимонной кислоты (10%) или соком лимона, коричневый – аммиаком, углекислым аммонием.
Нужно помнить, что порой слой патины придает монетам более благородный и винтажный вид, поэтому удалять его желательно не всегда. Некоторые, напротив, стараются искусственно состарить деньги домашним способом. Для этого надо взять литр дистиллированной воды, 5 г аптечной марганцовки, 50 г медного купороса. Раствор нагреть, не кипятя, бросить в него монеты, оставить до достижения нужного оттенка. Для закрепления эффекта высохшие деньги обработать смесью бензола и спирта (1:1). После монеты обретут красивый состаренный облик и смогут украсить любую коллекцию предметов антиквариата.
Чистка монет из меди
Медные монеты представляют собой антиквариат, и в наше время не выпускаются. Нередко их приходится чистить, чтобы вернуть привлекательный вид. Если монета контактировала со свинцом, налет на ней может быть желтоватым. В таком случае он прекрасно очищается столовым уксусом (9%). Зеленый налет убирают раствором лимонной кислоты (10%) или соком лимона, коричневый – аммиаком, углекислым аммонием.
Нужно помнить, что порой слой патины придает монетам более благородный и винтажный вид, поэтому удалять его желательно не всегда. Некоторые, напротив, стараются искусственно состарить деньги домашним способом. Для этого надо взять литр дистиллированной воды, 5 г аптечной марганцовки, 50 г медного купороса. Раствор нагреть, не кипятя, бросить в него монеты, оставить до достижения нужного оттенка. Для закрепления эффекта высохшие деньги обработать смесью бензола и спирта (1:1). После монеты обретут красивый состаренный облик и смогут украсить любую коллекцию предметов антиквариата.
Сварка меди и её сплавов со сталью. Как сваривать медь и сталь
На практике сварка меди и стали, чаще всего, осуществляется в стыковых соединениях. В зависимости от характера конструкции, швы в таком соединении могут быть наружными и внутренними.
Для сварки латуни со сталью лучше всего подходит газовая сварка, а для сварки красной меди со сталью — электродуговая сварка металлическими электродами.
Хорошие результаты также получаются при сварке угольными электродами под слоем флюса и газовая сварка под флюсом БМ-1. Часто на практике выполняют газовую сварку латуни со сталью, используя медь в качестве присадочного материала.
Подготовку сварных кромок при одинаковой толщине цветного металла и стали выполняют так же, как и при сварке чёрных металлов.
Сварку листов, толщиной менее 3мм выполняют без разделки, а листов, начиная с 3мм — со скосом кромок.
При недостаточном скосе кромок, или при наличии загрязнений на торцах свариваемых деталей, хорошего провара добиться невозможно. Исходя из этого, при сварке деталей больших толщин, в которых выполнена Х-образная разделка, притупление делать не следует.
Сварка меди со сталью — задача сложная, но вполне выполнимая для наплавочных работ и сварки, например, деталей химической аппаратуры, медного провода со стальной колодкой.
Качество сварки таких соединений удовлетворяет требованиям, предъявляемым к ним. Прочность меди можно повысить путём введения в её состав до 2% железа. При большем количестве железа прочность начинает падать.
При сварке угольным электродом необходимо применять постоянный ток прямой полярности.
Напряжение электрической дуги равно 40-55В, а её длина, примерно, 14-20мм. Сварочный ток выбирается в соответствии с диаметром и качеством электрода (угольный или графитовый) и составляет в пределах 300-550А. Флюс используют такой же, как и для сварки меди, состав этих флюсов дан на этой странице.
Вводят флюс в зону сварки, засыпая его в разделку.
Наилучшие результаты при сварке медных шин со стальными получаются при сварке «в лодочку». Схема такой сварки показана на рисунке. Вначале выполняется подогрев медных кромок угольным электродом, а затем сварка с определённым положением электрода и присадочного прутка (см. рисунок). Скорость сварки составляет 0,25м/ч. Сварка меди с чугуном производится с помощью таких же технологических приёмов.
Приварку низколегированной бронзы малой толщины (до 1,5мм) к стали толщиной до 2,5мм можно осуществить внахлёст неплавящимся вольфрамовым электродом в среде аргона на автомате с подачей присадочной проволоки диаметром 1,8мм со стороны.
При этом очень важно направить дугу на нахлёстку со стороны меди. Режимы такой сварки: сила тока 190А, напряжение дуги 11,5В, скорость сварки 28,5м/ч, скорость подачи проволоки 70м/ч. Медь и латунь хорошо свариваются со сталью стыковой сваркой с оплавлением
Медь и латунь хорошо свариваются со сталью стыковой сваркой с оплавлением.
При таком способе сварки стальные кромки оплавляются достаточно сильно, а кромки цветного металла незначительно. Учитывая это обстоятельство, и принимая в расчёт разность удельных сопротивлений этих металлов, принимают вылет для стали, равный 3,5d, для латуни 1,5d, для меди 1,0d, где d — диаметры свариваемых стержней.
Для стыковой сварки таких стержней методом сопротивления рекомендуют вылет, равный 2,5d для стали, 1,0d для латуни и 1,5d для меди. Удельное сопротивление осадки принимается в пределах 1,0-1,5 кг/мм2.
На практике часто возникает необходимость приварки шпилек диаметром 8-12мм из меди и её сплавов к стали, или стальных шпилек к медным изделиям.
Такую сварку осуществляют на постоянном токе обратной полярности под мелким флюсом марки ОСЦ-45 без предварительного подогрева.
Хорошо привариваются к стали или чугуну медные шпильки диаметром до 12мм или шпильки из латуни марки Л62, диаметром до 10мм при силе тока 400А.
А шпильки из латуни марки ЛС 59-1 для приварки не используют.
Стальные шпильки к медным и латунным изделиям привариваются плохо.
1 Что такое коррозия металлов и сплавов?
В целом этот процесс проявляется как разрушение материала в результате его взаимодействия с внешней средой. Причем ему подвержены как металлы, так и неметаллы (керамика, дерево, полимеры и т. д.). Сюда же мы можем отнести и старение резины, и разрушение пластика. Что же насчет металлических сплавов, так в этом случае наиболее явным примером коррозии является всем известная ржавчина.
Основной причиной данного явления служит недостаточная термодинамическая устойчивость того либо иного материала к каким-либо веществам, которые мы можем обнаружить в контактирующей среде. Так, например, резиновые покрытия портятся из-за взаимодействия с кислородом, полимеры разрушаются после многочисленных контактов с атмосферными осадками, а на большинство металлов и их сплавов губительно влияет чрезмерная влажность. Кроме того, значительно на скорость протекания процесса влияет и температура окружающей среды, в основном, чем данный параметр выше, тем скорее осуществляется разрушение.
Как обычное железо превращается в «нержавейку»
Чтобы получить металл с высокими антикоррозионными характеристиками, в него добавляют другие элементы: хром, никель, молибден, кремний, ванадий, вольфрам и другие, в разных пропорциях и количествах. Именно от пропорций зависят как физические, так и внешние характеристики полученного материала.
Железо с присадками называется легированным, различают низко-, средне-, высоколегированное.
В настоящее время особой популярностью пользуются 3 типа «нержавеек»:
- аустенитные с хромом и никелем, наиболее распространённые, в том числе при производстве перил, лестничных ограждений и поручней (сюда относится 300 серия);
- мартенситные с углеродом, более прочные, менее гибкие, сильнее подверженные коррозионному разрушению;
- ферритные, помягче мартенситных, а потому более простые в использовании, из них часто делают бытовые приборы (а сюда относится 400 серия).
Резюмируя: нержавеющие свойства металл получает при добавлении к нему различных присадок.
Коррозийные свойства меди
Медь – металл с высокими пластическими свойствами, имеющий красно-золотистый цвет, а после удаления оксидной пленки – чуть розоватый. По электропроводности он уступает лишь серебру, также характеризуется высокой теплопроводностью. Благодаря низкому удельному сопротивлению медь применяется в электротехнике: идет на изготовление медных пластинок, проволоки, обмотки двигателей.
Из-за высоких антикоррозионных качеств металл включается в сплавы для улучшения их технических характеристик (бронза, латунь и другие). В гальванической среде медь становится катодом, вступает в электрохимические процессы и вызывает ускоренное ржавление прочих металлов.
Медь – неактивный химический элемент, поэтому практически не взаимодействует с воздухом, водой (пресной, морской). Если воздух сухой, на поверхности материала формируется оксидная пленка толщиной до 50 мн. Медное изделие темнеет, становится коричневым или зеленоватым, это называется патиной. В ряде случаев патина воспринимается как декоративное покрытие. Интенсивность коррозии низкая при контакте с разбавленной соляной кислотой, но при реакции с рядом иных кислот, с галогенами, «царской водкой» металл окисляется с образованием карбоната меди.
Историческая справка, характеристика меди
Медь относится к отряду основных химических элементов. В естественном (чистом) виде это металл с красно-оранжевым оттенком. Его используют для изготовления очень большого ряда изделий, к которым относятся провода электрические, посуда, трубы, радиаторы автомобилей и т. п.
Информация археологов говорит о том, что медь начали использовать более десяти тысяч лет назад. Так медный кулон, обнаруженный в северных районах современного Ирака, был изготовлен около 8700 года до нашей эры.

Медь обладает высокими показателями тепловой и электрической проводимости, легко обрабатывается как горячим, так и холодным способом. У нее очень высокая коррозийная стойкость. Это обусловлено тем, что медь создает на своей поверхности очень тонкий оксидный защитный слой в результате реакции ее с кислородом.
Медь нашла широкое применение в производстве акустических, электрических и иных проводов, присутствуя там как металл высокой чистоты либо с небольшими добавлениями серебра, мышьяка, фосфора, теллура, серы.
Химические свойства хрома
Хром — элемент VIB группы таблицы Менделеева. Электронная конфигурация атома хрома записывается как 1s 22s 22p 63s 23p63d54s1, т.е. в случае хрома, также как и в случае атома меди, наблюдается так называемый «проскок электрона»
Наиболее часто проявляемыми степенями окисления хрома являются значения +2, +3 и +6. Их следует запомнить, и в рамках программы ЕГЭ по химии можно считать, что других степеней окисления хром не имеет.
При обычных условиях хром устойчив к коррозии как на воздухе, так и в воде.
Взаимодействие с неметаллами
с кислородом
Раскаленный до температуры более 600 oС порошкообразный металлический хром сгорает в чистом кислороде образуя окcид хрома (III):
4Cr + 3O2 =ot=> 2Cr2O3
с галогенами
С хлором и фтором хром реагирует при более низких температурах, чем с кислородом (250 и 300 oC соответственно):
2Cr + 3F2 =ot=> 2CrF3
2Cr + 3Cl2 =ot=> 2CrCl3
С бромом же хром реагирует при температуре красного каления (850-900 oC):
2Cr + 3Br2 =ot=> 2CrBr3
С азотом металлический хром взаимодействует при температурах более 1000 oС:
2Cr + N2 =ot=> 2CrN
с серой
С серой хром может образовывать как сульфид хрома (II) так и сульфид хрома (III), что зависит от пропорций серы и хрома:
Cr + S =ot=> CrS
2Cr + 3S =ot=> Cr2S3
С водородом хром не реагирует.
Взаимодействие со сложными веществами
Взаимодействие с водой
Хром относится к металлам средней активности (расположен в ряду активности металлов между алюминием и водородом). Это означает, что реакция протекает между раскаленным до красного каления хромом и перегретым водяным паром:
Взаимодействие с кислотами
Хром при обычных условиях пассивируется концентрированными серной и азотной кислотами, однако, растворяется в них при кипячении, при этом окисляясь до степени окисления +3:
В случае разбавленной азотной кислоты основным продуктом восстановления азота является простое вещество N2:
Хром расположен в ряду активности левее водорода, а это значит, что он способен выделять H2 из растворов кислот-неокислителей. В ходе таких реакций в отсутствие доступа кислорода воздуха образуются соли хрома (II):
При проведении же реакции на открытом воздухе, двухвалентный хром мгновенно окисляется содержащимся в воздухе кислородом до степени окисления +3. При этом, например, уравнение с соляной кислотой примет вид:
4Cr + 12HCl + 3O2 = 4CrCl3 + 6H2O
При сплавлении металлического хрома с сильными окислителями в присутствии щелочей хром окисляется до степени окисления +6, образуя хроматы:
При каких условиях начинается разрушение алюминия на воздухе
Вам будет интересно:Альтернативность — это наличие выбора возможностей
Некоторые интересуются, ржавеет ли алюминий на воздухе. Если будет разрушена оксидная пленка на верхнем слое металла, то может начаться процесс коррозии. В результате может проявиться ржавчина. Рост пленки, как правило, замедляется на свежем воздухе. Следует помнить, что оксид алюминия отличается хорошей сцепкой с поверхностью металла.
Если лист хранится на складе, то пленка будет от 0,01 до 0,02 мкм. Если металл соприкасается с сухим кислородом, то толщина оксидной пленки на поверхности будет от 0,02 до 0,04 мкм. Если алюминий подвергают термической обработке, то толщина пленки изменяется. Она будет равна 0,1 мкм.
Считается, что алюминий обладает достаточной стойкостью, чтобы использовать его на свежем воздухе. Например, его применяют в сельской местности, а также в удаленных промышленных зонах.
Коррозийные свойства
В связи с отсутствием у меди химической активности, при контакте с водой, влажным воздухом ее коррозия практически не возникает. Находясь в сухом воздухе, у металла может образовываться небольшая оксидная пленка толщиной до 50 нм. Если изделие лужено, то пленка почти не образовывается. Качественное покрытие из олова способно надежно защитить от влаги, перепадов температуры. При этом продолжительность эксплуатации такого предмета может составлять до 100 лет без потери первоначальных свойств. С течением времени цвет не будет изменяться. Применение луженных поверхностей давно показало себя с лучшей стороны. Примером могут стать купола множества храмов.
В связи с высоким порогом коррозийной стойкости медь активно применяется во многих химических и электрохимических производствах. К примеру, процесс обмеднения металла помогает решить множество задач при обработке. В одной из прошлых статей, мы рассматривали процедуру в домашних условиях, рекомендуем ознакомиться.
Что такое коррозия металлов и сплавов
Под коррозией понимают процесс разрушения металла под действием агрессивных факторов окружающей среды. В той или иной степени ржавеют все металлы, сплавы, в результате чего на них появляются ржавчина и участки нарушения целостности (дыры). Портиться со временем способны и неметаллы: примером можно назвать старение резины или пластика от взаимодействия с кислородом, при частых контактах с водой, перепадами температур.
Основной причиной коррозии считается термодинамическая неустойчивость металла к влиянию физических факторов или химических веществ, которые присутствуют в контактной среде. По сравнению с железом медь окисляется намного меньше, но при увеличении температуры этот процесс значительно ускоряется. При регулярном нахождении в среде с температурой выше +100 градусов любой металл ржавеет в несколько раз быстрее.
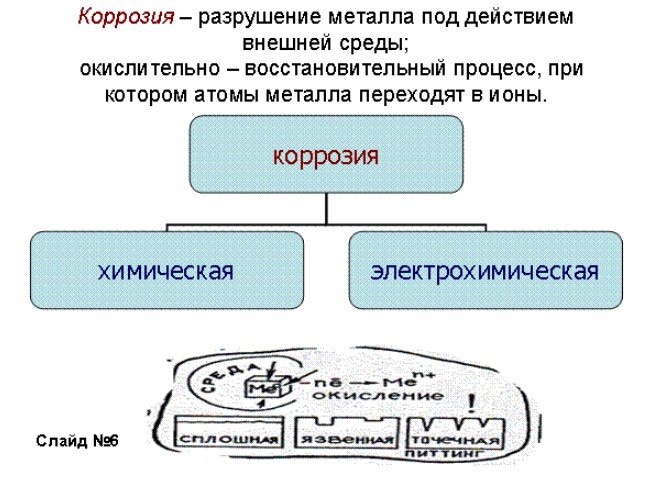
Нахождение в почве и влажном воздухе
Коррозия меди в почве, в основном, вызывается влиянием кислот, которые содержатся в грунте. Если сравнить с воздействием воды, то кислород в грунте значительно меньше окисляет металлические элементы. К наиболее опасным в почве относятся микроорганизмы, вернее, их выделения. Зачастую они способны выделять сероводород, разрушающий металл. Так, медь длительно пролежавшая в почве способна полностью разложиться.
Во влажном воздухе процесс протекает не стремительно. Необходимо длительное время. В сухом климате можно вообще не наблюдать разрушительных влияний. Объясняется это тем, что во влажном воздухе высока концентрация углекислого газа, сульфидов, хлоридов, вызывающих коррозию и разрушительных для защитной пленки.
Длительное пребывание на влажном воздухе способно вызывать образование слоя патины. Так называется зеленый налет на меди. Она представляет собой оксиды солей, которые на начальном этапе темно-коричневого цвета, а затем поверхность начинает зеленеть. Особенностью патины является то, что ее невозможно растворить в воде и на нее не действует повышенная влажность воздуха. Она имеет нейтральные свойства к самой меди, что позволяет ей защищать поверхность от пагубного влияния окружающей среды. Кроме этого современные методы создания искусственной патины позволяют ее использовать в предметах искусства и при реставрации.
Посмотрите личный опыт борьбы с коррозийными очагами с помощью ингибиторов.
Новые бессвинцовые сплавы
Допустимое содержание свинца в питьевой воде в Германии составляет не более 10 мкг/л. Этот показатель был утверждён немецким правительством в 2013 году. Что интересно, ещё в 2003 году данная норма находилась на уровне 25 мкг/л. За 10 лет борьба со свинцом в Германии стала более жесткой и его норма в питьевой воде снизилась на 15 пунктов, то есть с 25 до 10 мкг/л.
Ограничение нормы содержания свинца в питьевой воде затронуло все немецкие производственные предприятия, занимающиеся изготовлением продукции для систем питьевого водоснабжения. Они были вынуждены отказаться от большей части латуни с содержанием свинца, и дружно перешли на бессвинцовые сплавы, их называют Pb-free. С 2013 года сантехническая арматура от труб до фитингов, производящаяся в Германии для водопроводных нужд, практически не содержит свинец.

Не смотря на то, что свинец в Западной Европе стал «персоной нон грата», небольшая доля этого металла все-таки необходима для сохранения механических свойств в ходе обработки латуни. Оставить свинец в некоторых сантехнических изделиях помогли новые сплавы, разработанные в Германии по стандарту DIN 50930-6. Его приняли 1 августа 2001 года с обозначением: «Коррозия металлических материалов под воздействием воды внутри труб, резервуаров и приборов». Уже тогда, согласно нормативу DIN 50930-6, немцы начали искать и разрабатывать новые сплавы со сниженным содержанием свинца, чтобы они заменили устаревшую латунь с содержанием токсичного металла.
За последние годы европейские металлурги значительно увеличили производство сплавов Pb-free и бессвинцовой латуни, которая стала пользоваться большим спросом не только в Германии, но и других странах Европы
Потребители Pb-free обратили внимание, что сплав имеет более высокие технические свойства, чем латунь с множеством примесей. Например, бессвинцовый сплав более устойчив к воздействию соленой морской воды
Он совершенно безопасен и может использоваться в системах питьевого водоснабжения. Кроме того, бессвинцовая латунь нашла широко применение в производстве деталей для телекоммуникаций, бытовой техники, электроники, коннекторов (электрических соединителей) и другой аппаратуры.
Бессвинцовую или простую латунь также называют «двойной», так как она содержит всего два компонента – медь и цинк. Как правило, двойную латунь маркируют буквой «Л» и цифрой, которая обозначает процентное содержание меди: Л63, Л68, Л75, Л80, Л85, Л90, Л96. В тоже время, доля цинка в простой латуни определяется по остатку на 100%. Если в сплаве Л96 содержится 96% меди, то оставшиеся 4% — это цинк.
Необходимо отметить, что изъятие из латуни свинца осложнило процесс обработки и резки сплавов Pb-free. Небольшое количество свинца добавлялось в латунь для того, чтобы обеспечить наилучшую обработку металла при резке. Отсутствие Pb повлекло за собой революционные изменения устоявшегося за годы технологического процесса. Европейским предприятиям пришлось задуматься над усовершенствованием оборудования, отвечающего за обработку и резку сплавов Pb-free. Потребовалось разработать новые технологии, модернизировать режущие инструменты, наладить новое оборудование, переобучать мастеров и дополнительно повышать их профессиональный уровень. Трудоемкость обработки бессвинцовой латуни значительно увеличилась, соответственно возросла себестоимость изготовления изделий из сплавов Pb-free. По сравнению с изделиями из свинцовой латуни стоимость бессвинцовых аналогов в 2-3 раза выше.
Окисленная медь
Окисленная медь содержит в себе много кислорода, что нежелательно. Для восстановления закиси меди в расплавленный металл вводят древесину. Газообразные продукты сгорания, проходя через металл, перемешивают его.
Окисленную медь восстанавливают в токе водорода при той же температуре. Полное удаление кислорода таким путем не достигается.
Окисленную медь восстанавливают водородом.
Окисленную медь растворяют в серной кислоте и далее процесс проводят, как описано на стр.
Окисленную медь восстанавливают водородом.
Окисленную медь дробят на кусочки длиной 3 — 4 мм и загружают в трубку для сожжения.
Для окисленной меди, однако, интерференционные данные всего лишь на 20 % меньше, чем данные по адсорбции пальмитиновой кислоты.
Если внести окисленную медь в восстановительную зону пламени бунзеновской горелки ( верхняя часть конуса), то оксид восстановится водородом, и мы увидим, что чистый металл красного цвета.
Осаждение никеля на окисленную медь проводилось из электролита Уотта при рН 5 2 — 5 3, причем ток включался не сразу после погружения образца, а через 4 мин. Федера , значительная часть окиси ( — 350 А) растворяется, причем образовавшиеся ионы меди со-осаждаются с первым слоем никеля, образуя сплав медь — никель. При включении тока происходит также электрохимическое восстановление окиси. В случае тонких окисных пленок ( 650 А при включении тока или 1000 А перед погружением в электролит) вся окись восстанавливается. Более толстые пленки остаются под никелем.
После удаления шлака для раскисления частично окисленной меди в расплав бросают сырые березовые чурки, которые при температуре печи образуют пары воды, водород и окись углерода.
|
Распределение по направлениям коэффициента отражательности черной окисленной меди.| Приведенная характеристика отражательности различных материалов для падающей черной радиации. а — еловое дерево ( пад 910 С. Ь — стеатит Спад 905 С. с — белая бумага СПад 905 с. d — белая бумага Опад 535 С. е — черная окисленная медь. |
На рис. 181 показан коэффициент отража-тельности окисленной меди для различных углов падающего излучения и температуры источника черного излучения.
Следовательно, выщелачиванию серной кислотой подлежат только руды окисленной меди, не содержащие в значительных количествах растворимых в серной кислоте соединений трехвалентного железа, карбонатов и основных солей.
Изучая под электронным микроскопом структуру порошков чистой меди, окисленной меди и чистой меди, покрытой тонким слоем нитрованного масла, Е. С. Чуршуков установил, что нитрованное масло придает меди структуру, аналогичную окисленной меди. Таким образом, прямым наблюдением было показано, что нитрованное масло способно вызывать явление анодной пассивности меди со сдвигом потенциала в сторону положительных значений.
По-видимому, разумно предположить, что в системе присутствует или может образоваться некоторое количество окисленной меди.
Кабели из катодной меди: применение
Современная кабельная продукция, сделанная с использованием бескислородной меди, отличается повышенной проводимостью. Это дает возможность осуществлять высокую пропускную способность электрических сигналов при меньших сечениях проводов.
Однако стоит отметить, что широкого использования кабели из бескислородной меди не нашли. А все потому, что провода из этого металла отличаются высокой стоимостью. Для достижения нужных параметров используют простые медные с большим диаметром, предпочитая не тратиться на дорогие изделия из бескислородной меди.
Но есть и области, в которых предпочтение отдается высокой проводимости в сочетании с небольшим диаметром проводов. Это необходимо для обеспечения в том числе эстетичного вида. К таким сферам относятся производство музыкального оборудования, качественных наушников, а также те, где надо получить устройства, воспроизводящие высококачественные звуки профессионального уровня.
При применении такой меди отмечаются ее достоинства в противостоянии внутренней коррозии. Благодаря этому свойству провода из бескислородной меди со временем характеристик своих не теряют. По этой причине кабели с начинкой из этого металла используют в условиях, где присутствует высокая влажность.
Что такое коррозия металлов и сплавов
Под коррозией понимают процесс разрушения металла под действием агрессивных факторов окружающей среды. В той или иной степени ржавеют все металлы, сплавы, в результате чего на них появляются ржавчина и участки нарушения целостности (дыры). Портиться со временем способны и неметаллы: примером можно назвать старение резины или пластика от взаимодействия с кислородом, при частых контактах с водой, перепадами температур.
Основной причиной коррозии считается термодинамическая неустойчивость металла к влиянию физических факторов или химических веществ, которые присутствуют в контактной среде. По сравнению с железом медь окисляется намного меньше, но при увеличении температуры этот процесс значительно ускоряется. При регулярном нахождении в среде с температурой выше +100 градусов любой металл ржавеет в несколько раз быстрее.
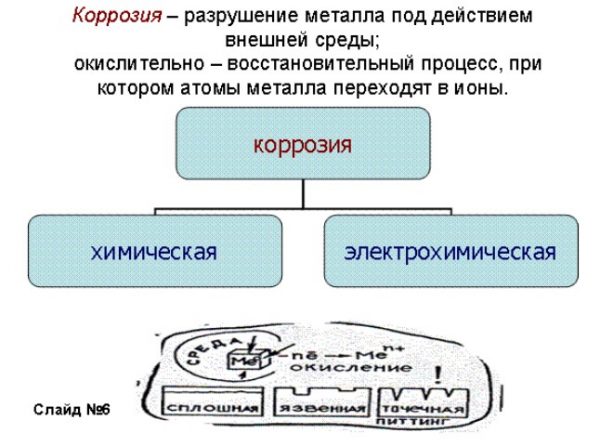
Коррозия луженой меди
Луженая медь отличается превосходной коррозионной стойкостью. Луженая медь отлично служит даже под воздействием дождя, града, снега, не чувствительна к перепаду температуры окружающей среды. Атмосферная коррозия луженой меди весьма незначительна. Оловянное покрытие по отношению к меди является анодом, т.к. имеет более электроотрицательный потенциал. Если на нем нет никаких изъянов (пор, трещин, царапин), через которые медь контактирует с атмосферой – оно прослужит очень долго. Если же дефекты покрытия присутствуют – атмосферная коррозия луженой меди протекает по следующим реакциям:
А: Sn – 2e→ Sn 2+ – окисление олова;
К: 2 H2О + O2 + 4e → 4 OH – – восстановление меди.
Качественное оловянное покрытие продлевает срок службы луженой меди до 100 лет и более.